Herzrhythmus – die Akademie
Herzrhythmusstörungen sind nicht selten und können ganz unterschiedlicher Ursache haben. Die Bandbreite reicht vom gelegentlichen Extraschlag bis hin zum potenziell tödlichen Kammerflimmern. Gar nicht so leicht also, zu verstehen, ob das eigene Leiden einfach nur lästig oder (auf Dauer) vielleicht sogar lebensbedrohend ist. Und unabhängig vom Schweregrad der Erkrankung zeigt unsere Erfahrung:
Wer versteht, was in seinem Körper vor sich geht, muss weniger Ängste ertragen und fühlt sich wohler. Daraus ist unsere Herzrhythmus-Akademie entstanden. Sie bietet Ihnen einen lexikonartigen Einblick in das weitreichende und medizinisch spannende Thema Herzrhythmus – und schenkt Ihnen Sicherheit.
Diagnostik von Herzrhythmusstörungen
Für die Beurteilung einer Herzrhythmusstörung ist fast immer eine umfassende Ursachendiagnostik nötig. Dazu gehört u.a. die Abklärung einer strukturellen Herzerkrankung wie:
• die koronare, also gefäßbezogene, Herzerkrankung
• ein Herzklappendefekt oder
• die Erkrankung des Herzmuskels
Im jungen Lebensalter haben Herzrhythmusstörungen nicht selten eine genetische Ursache.
Eine sorgfältige Anamnese liefert schon bis zu 80% der Diagnose und ist deshalb ganz besonders wichtig. Dazu nutzen wir seit vielen Jahren erfolgreich einen 12 Fragen-Katalog, den Sie bitte vor Ihrem Besuch unserer Rhythmussprechstunde vorab beantworten.
Diagnostik
Elektrokardiogramm
Das Elektrokardiogramm (syn. Standard-EKG, 12-Kanal- EKG) ist seit über 100 Jahren der Standard in der Diagnostik von Herzrhythmusstörungen. Die EKG-Diagnostik ist leicht verfügbar und schnell und wiederholt durchführbar. Die meisten Rhythmusstörungen können damit erkannt und klassifiziert werden. Das EKG gibt Hinweise zum Ursprungsort der Arrythmie und ihrem potenziellen Schweregrad. In Kombination mit der Anamnese können nach fachkundiger Sichtung des EKG erste therapeutische Entscheidungen getroffen werden.
Weniger gut geeignet ist das Ruhe-EKG bei der Dokumentation sporadischer Arrhythmieepisoden. Sehr viel besser sind Methoden, die über einen längeren Zeitraum den Herzrhythmus kontinuierlich aufzeichnen, oder bedarfsweise aktiviert werden können:
Das Langzeit-EKG (syn. Holter-EKG, 24-Stunden-EKG) ermöglicht die dauernde Überwachung des Herzrhythmus über einen Zeitraum von meistens 24-72 Stunden – mit modernen Geräten sogar über eine Woche und länger.
Wichtig dabei ist die sorgfältige Führung eines Journals, in dem Symptome, aber auch Schlafphasen, Belastungen, Medikamenteneinnahme etc. protokolliert werden. Das hilft dem Arzt bei der Auswertung des EKG, eventuelle Rhythmusstörungen besser klassifizieren zu können. Das Patientenjournal für ein Holter-EKG können Sie sich hier gern herunterladen.
Als Patient des RHYTHMOLOGICUM garantieren wir Ihnen, dass wir Ihr Holter-EKG nicht – wie häufig üblich – von einem externen Provider bewerten lassen. Die Auswertung erfolgt bei uns persönlich über unser Ärzte-Team, um nicht Gefahr zu laufen, kontextbezogene Informationen ggf. zu verlieren.
Ereignis-EKG (syn. Event-Rekorder, Loop-Rekorder). Diese Geräte erlauben es, Herzrhythmusstörungen in vorher definierten Herzfrequenzzonen über einen noch längeren Zeitraum und bis zu 4 Wochen festzuhalten.
Eine gute Alternative für anfallsweise, symptomatische Herzrhythmusstörungen sind sogenannte patientenaktivierte Ereignisrekorder.
Die Firma Apple leistete mit der möglichen EKG-Aufzeichnung in der Apple Watch seit der Version 4 Pionierarbeit. So ist die Apple Smartwatch in den USA und Europa inzwischen auch als Medizinprodukt zugelassen und spielt ihre Stärke besonders bei der Feststellung von Vorhofflimmern aus.
Außerhalb der iOS-Welt sind Smartwatches von Withings®, Samsung® und Fitbit® gute und zertifizierte Alternativen. Weitere Hersteller werden sicher folgen.
Implantierbare
Event-Recorder
(„Loop“-Rekorder)
Diese leicht und unkompliziert implantierbaren kleinen Geräte können den Herzrhythmus über mehrere Jahre hinweg kontinuierlich aufzeichnen.
Sie eignen sich besonders bei Verdacht auf sehr seltene, aber mit hoher Gefährdung einhergehenden Herzrhythmusstörungen – wie zum Beispiel plötzliche Ohnmachtsanfälle mit Verletzungspotenzial durch einen Sturz oder zur Suche nach Vorhofflimmern bei ungeklärtem Schlaganfall.
Elektrophysiologische Untersuchung (EPU)

Eine Rolle spielt die diagnostische EPU gelegentlich noch zur Sicherung der Indikation von Herzschrittmacherimplantationen und zur Charakterisierung des Risikos für den plötzlichen Herztod.
Unter lokaler Anästhesie und allgemeiner Sedierung („Schlafnarkose“) werden über ein Blutgefäß in der Leistenregion Zugänge (Schleusen) platziert, über die ein bis zwei (selten mehrere) dünne Katheter in das Herz vorgeschoben werden. Die Katheter ermöglichen die Ableitung elektrischer Signale aus verschiedenen Herzhöhlen mit einer hohen Präzision im Bereich weniger Millisekunden. Durch elektrische Stimulation können die physiologischen und pathophysiologischen Leitungseigenschaften des Herzmuskels und des spezifischen Reizleitungssystems charakterisiert und eventuelle Herzrhythmusstörungen ausgelöst beziehungsweise beendet werden. Oft kann durch die Gabe kurzwirksamer Medikamente die Auslösbarkeit von Arrhythmien zusätzlich beeinflusst werden.
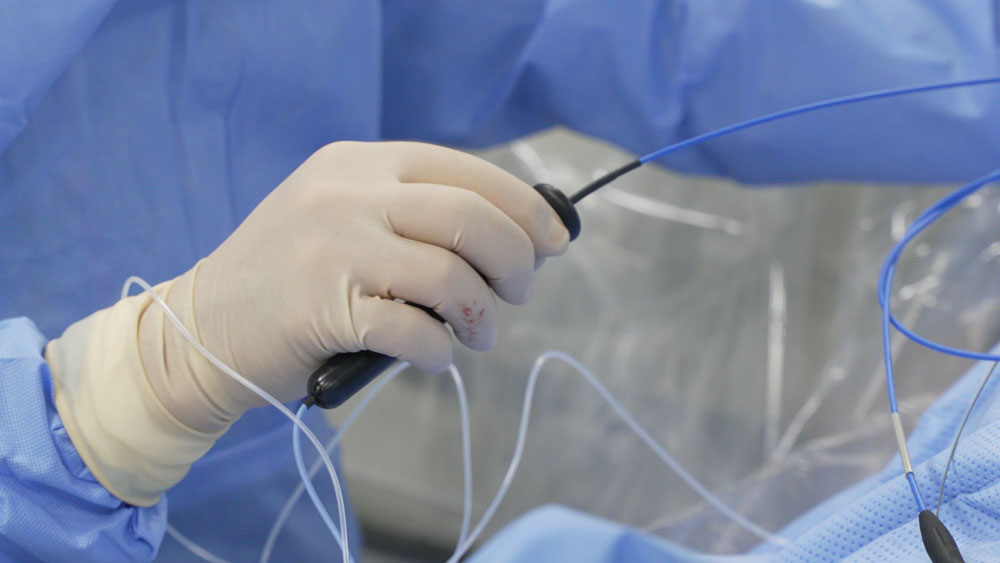
Eine diagnostische EPU dauert selten länger als 20 bis 45 Minuten und ist – auch wenn es auf den ersten Blick vielleicht anders aussieht – ein sehr komplikationsarmer Eingriff.
Geht es um die Abklärung kardiovaskulärer Begleiterkrankungen, die eine entscheidende Rolle in der Beurteilung von Herzrhythmusstörungen spielt, sind neben der reinen Rhythmusdiagnostik weiterführende Untersuchungen im RHYTHMOLOGICUM möglich:
Dazu gehören in erster Linie Ultraschallverfahren, Ergometrie und labormedizinische Analysen.
Transthorakale Echokardiografie
(syn. Herzultraschall, „Echo“))
Die transthorakale Echokardiografie (TTE) ist ein seit Jahrzehnten etabliertes Verfahren zur Beurteilung der Anatomie und der Funktionsweise des Herzens. Sie ist eine äußerliche nichtinvasive, schmerzfreie und jederzeit reproduzierbare Untersuchung. In der Rhythmologie werden vor allem die Pumpkraft (Ejektionsfraktion bzw. EF), Klappenfunktionsstörungen, Dimensionen der Herzhöhlen und regionale (segmentale Wandbewegungsstörungen) für die Klassifizierung und die Prognose von Arrhythmien benötigt.
Eine Echokardiografie dauert je nach Fragestellung gerade einmal zwischen 5-15 Minuten.
Spezielle elektrophysiologische Fragestellungen betreffen insbesondere die Pumpfunktion der Herzkammern, die Größe und Funktion der Vorhöfe und Fehlfunktionen der Herzklappen.
Transösophageale Echokardiografie
(syn. „Schluckecho“)
Auch diese Untersuchungstechnik wird schon seit vielen Jahren in der Kardiologie erfolgreich eingesetzt. In der Rhythmologie ist ihre Domäne vor allem der Ausschluss von Blutgerinnseln im linken Vorhof in der Vorbereitung einer Vorhofflimmer-Ablation. Ein TEE, besser bekannt als Schluck-Echo, kann mit 99%-iger Sicherheit einen Thrombus ausschließen und damit die Sicherheit der Vorhofflimmer-Ablation erhöhen.
Die Untersuchung wird unter einer Sedierung durchgeführt und hat bei Durchführung durch einen erfahrenen Kardiologen kaum Risiken.
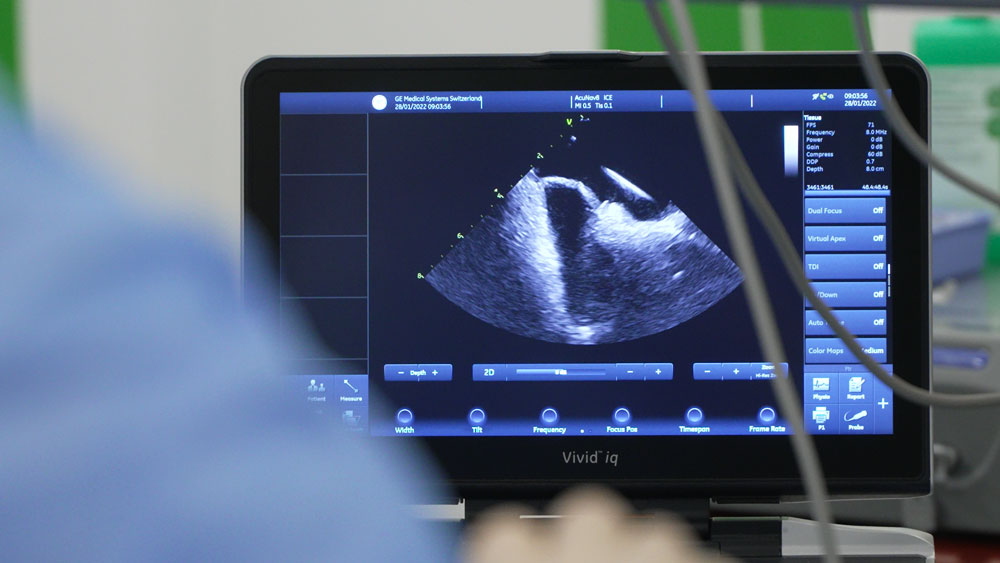
Intrakardiale Echokardiografie
Ein dünner, über die Leiste in das Herz vorschiebbarer Katheter ermöglicht einen direkten Blick auf wichtige kardiale Strukturen und die elektrophysiologischen Sonden. Diese selten durchgeführte Untersuchungstechnik wird durch uns gern bei komplexer Anatomie oder schwieriger Punktion der Vorhofscheidewand angewendet.
Ergometrie
Die Belastungs-EKG-Untersuchung ist aus der kardiologischen Diagnostik nicht mehr wegzudenken. Die Ergometrie ermöglicht in der rhythmologischen Diagnostik eine sehr zuverlässige Einschätzung des Herzfrequenzverhaltens in Ruhe aber auch während und nach einer körperlichen Belastung.
Die Belastung hat zusätzlich oft einen Einfluss auf die Auslösung einer Herzrhythmusstörung, wie z. B. bei der Diagnostik von Extraschlägen, die unter Belastung zunehmen aber auch gelegentlich verschwinden können.
Klassifizierung von Herzrhythmusstörungen
Klassifizierung
Bradykarde Herzrhythmusstörungen
Das Herz ist ein einzigartiges Organ. Im Laufe eines durchschnittlich 80-järigen Lebens schlägt es ohne Pause mehr als 3 Milliarden Mal. Dabei werden mehr als 250 Millionen Liter Blut durch den Blutkreislauf gepumpt.
Eine unglaubliche Leistung. Normalerweise nimmt man den Herzschlag nicht bewusst wahr. Erst durch Herzrhythmusstörungen, wie Extraschläge oder Aussetzer, spürt man sein Herz in der Regel.
Bradykardie: Physiologisch langsamer Herzschlag
Die Herzfrequenz schwankt im Ruhezustand in der Regel, je nach Größe des Herzens und dem individuellen Trainingszustand, zwischen 60 und 100/min. Bei besonders gut trainierten Menschen sind Herzfrequenzen unterhalb von 50/min eher die Regel.
Finden sich Herzfrequenzen in Ruhe auch ohne Ausdauersport unterhalb von 60/min, spricht man von einer Bradykardie. Diese ist noch längst kein Grund zur Sorge, sollte aber – insbesondere, wenn sie mit Beschwerden wie ungewöhnlicher Müdigkeit, Schwindel, Ohnmachtsanfällen oder Luftnot bei alltäglichen Belastungen einhergeht – abgeklärt und behandelt werden. Klinische Untersuchung, EKG, Langzeit-EKG, Belastungstest, Herzultraschall und Labortests helfen, die Diagnose einer Bradykardie zu sichern und mögliche Ursachen zu identifizieren. Gelegentlich sind schlafmedizinische Untersuchungen oder Kipptischuntersuchungen für bestimmte Formen bradykarder Herzrhythmusstörungen angezeigt.
Die Einteilung bradykarder Herzrhythmusstörungen ist auf vielerlei Weise möglich. Wir bevorzugen einen pragmatischen und praxisnahen Ansatz:
Reversible („umkehrbare“) Ursachen
Dazu gehören
• Nebenwirkungen von Medikamenten (Schlafmittel, Opioide, Antidepressiva und Antipsychotika, Blutdruckmittel und antiarrhythmische Medikamente)
• Unterfunktion der Schilddrüse
• Störungen des Elektrolyt- („Blutsalz“-) Haushalts
• Entzündliche Erkrankungen (Rheumatoide Arthritis, Lupus)
• Schlafbezogene Atemstörungen (Schlaf – Apnoe – Syndrom)
Irreversible Ursachen
• Degenerative Erkrankungen des Herzmuskels und des Reizleitungssystems
• Genetische Erkrankungen kardialer Ionenkanäle
• Speicherkrankheiten des Herzens
• Erkrankung des Herzmuskels und gestörte Blutversorgung des Herzens
• Seltene Komplikation nach herzchirurgischer Operation oder perkutaner interventioneller Behandlung (Herzklappentherapie, Katheterablation)
Während bei den reversiblen Ursachen eine Behandlung der grundliegenden Störung die Bradykardie und ihre Symptome beseitigen kann, ist bei den irreversiblen Ursachen oft eine Schrittmacherimplantation nötig.
Bei den bradykarden Herzrhythmusstörungen unterschiedet man zwischen Funktionsstörungen der Impulsbildung und denen der Reizleitung des Herzens. Dazu ein kurzer Exkurs in die Elektroanatomie des Herzens:
Das Herz besteht aus vier Herzkammern. Die Impulsbildung (der Ursprung der elektrischen Aktivität) erfolgt im Normalfall im sogenannten Sinusknoten, der sich im hinteren oberen Abschnitt des rechten Vorhofs befindet. Über die Vorhofmuskulatur wird in sehr kurzer Zeit (ca. 0,1 s) der linke Vorhof erregt. Gleichzeitig erreicht der elektrische Stimulus auch die zweite wichtige Leitungsstruktur – den AV-Knoten (Atrioventrikulärer Knoten). Der AV-Knoten filtert wie ein Kondensator die elektrische Leitung und leitet im Normalfall elektrische Impulse nur bis zu einer maximalen Herzfrequenz weiter. Diese Verzögerung ist lebenswichtig und schützt die Hauptkammern vor hohen Herzfrequenzen – wie beim Vorhofflimmern oder Vorhofflattern – und damit vor potentiell tödlichen Kammerfrequenzen >250/min.
Die dritte Reizleitungsebene umfasst spezifische Leitungswege, die die elektrischen Impulse ausgehend vom AV-Knoten an die Arbeitsmuskulatur der Hauptkammern weitergeben (His-Bündel, Tawara-Schenkel, Purkinje-System)
Sinusknotenerkrankung
Neben den reversiblen Ursachen finden sich beim kranken Sinusknoten ursächlich häufig eine degenerative Erkrankung. Durch Alterungsprozesse wird das hochsensible Netzwerk der impulsbildenden Zellen durch Bindegewebeeinlagerung („Fibrose“) irreversibel geschädigt.
Das führt zu einer deutlichen Sinusbradykardie in Ruhe, inadäquatem Anstieg der Herzfrequenz bei Belastung („chronotrope Inkompetenz“) und begünstigt das Auftreten von Vorhofrhythmusstörungen wie Vorhofflimmern und Vorhofflattern (Brady-Tachy-Syndrom).
Bei Symptomen ist oft nur die Einpflanzung eines Herzschrittmachers langfristig hilfreich.
Überleitungsstörungen
Auch bei diesen bradykarden Rhythmusstörungen findet sich ursächlich oft eine degenerative Ursache. Die Symptome sind ähnlich wie bei der Sinusknotenerkrankung: Schwindel, Ohnmachtsanfälle (Synkopen), Luftnot bei körperlicher Belastung. Ist die Diagnose gesichert, kann auch hier die Herzschrittmacherimplantation ein beschwerdefreies Leben ermöglichen.
Die Einteilung der Überleitungsstörungen in AV-Block I-III Grades, bifaszikulärer (zwei Leitungsbahenen betroffen) oder trifaszikulär (drei Leitungsbahnen gestört), supra- oder infrahisär (oberhalb oder unterhalb des His-Bündels) ist medizinisch und prognostisch wichtig. Gerade bei älteren Patienten ist ein pragmatischer symptom- und ursachenbezogener Ansatz hilfreich.
Tachykarde Herzrhythmusstörungen
Ist die Herzfrequenz unabhängig von einer körperlichen Belastung anfallsweise oder dauerhaft höher als 100/min, spricht man von einer tachykarden Herzrhythmusstörung.
Sinustachykardie
Der Sinusrhythmus ist in der Lage, sich an den Aktivitätszustand des Menschen schnell und bedarfsgerecht anzupassen. Bei körperlicher Arbeit steigt der Sauerstoffbedarf der Muskulatur um ein Vielfaches. Das Herz kann diesen erhöhten Bedarf durch ein höheres Blutvolumen pro Herzschlag (Schlagvolumen) und noch viel mehr durch eine Steigerung der Herzfrequenz (Schläge/ min) decken. Während in Ruhe etwa 5l Blut durch den Kreislauf gepumpt werden, steigert sich dieser Wert auf das 6-fache unter hoher körperlicher Belastung.
Ist die Sinusfrequenz auch in Ruhe höher als 100/ min oder steigt sie unter leichterer körperlicher Anstrengung unverhältnismäßig schnell an, spricht man von einer inadäquaten oder nicht-physiologischen Sinustachykardie.
Ursachen einer nicht-physiologischen Sinustachykardie können vielfältig sein:
Kardiale Ursachen, also das Herz betreffend:
• Herzschwäche (“Herzinsuffizienz“)
• Herzinfarkt
• Herzmuskelerkrankungen
• Herzklappenerkrankungen (Mitralklappen-
oder Aortenklappen-Insuffizienz)
Extrakardiale Ursachen, also außerhalb des Herzens liegend:
• Sauerstoffmangel (durch Blutarmut = Anämie oder „dünne Luft“ in großer Höhe)
• Niedriger Blutdruck (z.B. bei Flüssigkeitsmangel, Dehydration)
• Fieber
• Hormonelle Erkrankungen (z.B. Schilddrüsenüberfunktion)
• Arzneimittel (z.B. adrenerge Substanzen wie in Asthmasprays oder Mittel gegen niedrigen Blutdruck)
• Genussmittel (Koffein, Nikotin und Alkohol)
• Drogen (Cannabis, Kokain, Amphetamine)
• Störungen des autonomen Systems
• Psychosomatische Erkrankungen
Sind kardiale Probleme ausgeschlossen und extrakardiale Ursachen eliminiert worden, die Sinustachykardie aber nach wie vor auftritt, kann es sich auch um eine Störung des autonomen Systems oder nicht selten um eine psychosomatische Erkrankung handeln.
Eine symptomatische medikamentöse Behandlung ist in der Regel erst bei einer umfassenden Ausschlussdiagnostik indiziert und hilfreich. Die Katheter-Ablation zur Behandlung einer Sinustachykardie ist bei uns eine selten notwendige Ausnahme.
Atriale Tachykardien (Vorhoftachykardien)
Diese Form der Herzrhythmusstörung ist relativ selten. Es kann sich um einen Fokus mit gesteigerter elektrischer Aktivität, um einen Mikrokreislauf oder einen Mechanismus mit einer Kreislauftachykardie handeln. Zunehmend häufiger werden atriale Tachykardien als Folge von Ablationen von Vorhofflimmern beobachtet.
Eine medikamentöse Therapie ist oft schwierig durchführbar und scheitert nicht selten an den Nebenwirkungen der verabreichten Medikamente. Die effektivste Behandlung ist eindeutig die Katheter-Ablation, die allerdings nicht immer beim ersten Versuch erfolgreich ist.
AV-Knoten-Reentrytachykardie (AVNRT)
Die AVNRT ist die häufigste tachykarde Herzrhythmusstörung bei jüngeren Menschen. Fast immer ist sie angeboren, gelegentlich findet sich eine familiäre Häufung. Der Tachykardie-Mechanismus beruht auf unterschiedlichen Leitungseigenschaften des zum AV-Knoten zuführenden Gewebes (langsamer und schneller Leitungsweg). Ausgelöst wird sie durch Extraschläge oder Salven von Extraschlägen.
Die Herzfrequenz liegt typischerweise bei jüngeren Patienten meist um 150/min. Der Beginn und das Ende werden als plötzlich beschrieben: „als ob man einen Schalter umlegen würde“.
Im Allgemeinen ist die AVNRT eine gutartige Rhythmusstörung. Aber es gibt bei bis zu 5% der Patienten die Möglichkeit, über einen körpereigenen Reflex plötzlich das Bewusstsein zu verlieren.
Aufgrund der Möglichkeit der kompletten Heilung dieser Rhythmusstörung in über 95% der Fälle empfehlen wir die Katheter-Ablation als die Therapie der Wahl für diese Rhythmusstörung.
AV-Reentrytachykardie (AVRT)
Häufigkeit und Symptomatik sind bei dieser Herzrhythmusstörung ganz ähnlich wie bei der oben beschriebenen AVNRT. Die Anfallsherzfrequenz ist meist etwas höher (nicht selten >200/min). Der Tachykardie-Mechanismus ist aber anders. Ursächlich ist eine in der Embryonalzeit bei der Entstehung des Herzens übriggebliebene Muskelbrücke zwischen Vorhof und Herzkammer. Auch hier können Extraschläge die Tachykardie „zünden“. 95% dieser Reentrytachykardien bei AVRT haben eine Aktivierung vom Vorhof auf die Herzkammer über den AV-Knoten und zurück über die zusätzliche Leitungsbahn (orthodrome AVRT). Nur bei 5% der Tachykardien findet sich ein umgekehrter Mechanismus (antidrome AVRT).
AVRT finden sich beim Wolf-Parkinson-White- (WPW-) Syndrom. Ganz selten, aber von hoher medizinischer Bedeutung, ist, dass über die Muskelbrücke zwischen Vorhof und Herzkammer, der die bremsende und schützende Eigenschaft des AV-Knotens fehlt, schnelle Vorhofrhythmusstörungen wie Vorhofflimmern ungehindert auf die Herzkammern übergeleitet werden und zu Synkopen oder sogar zum plötzlichen Herztod führen können. Aus diesem Grund empfehlen wir bei Patienten mit dieser Herzrhythmusstörung ebenfalls eine Katheter-Ablation als Methode der ersten Wahl.
Vorhofflattern
Nach dem Vorhofflimmern ist das Vorhofflattern die häufigste anhaltende Herzrhythmusstörung. Ähnlich wie beim Vorhofflimmern ist neben der eigentlichen Herzrhythmusstörung mit den möglichen Symptomen einer Tachykardie (Herzrasen, Schwindel, Leistungseinschränkung) die Gefahr eines Schlaganfalls durch Bildung von Blutgerinnseln im linken Vorhof deutlich erhöht.
Beim typischen Vorhofflattern kreist die Erregungsfront um die Trikuspidalklappe (Dreisegelklappe) zwischen rechtem Vorhof und rechter Herzkammer. Seltenere Formen treten nach Operationen oder Katheter-Interventionen auf. In diesen Fällen kreist die Erregung meist um narbige Bezirke.
Eine medikamentöse Behandlung zielt auf die Senkung der Herzfrequenz und den Schutz vor einem Schlaganfall.
Medikamente mit sicherer und effektiver Wiederherstellung des Herzrhythmus bzw. zur Prophylaxe des Vorhofflatterns sind gegenwärtig noch nicht verfügbar. Die Behandlung ist deshalb ebenfalls eine Domäne der Ablationstherapie und mit hoher Sicherheit und Effektivität (90%) durchführbar.
Vorhofflimmern
Vorhofflimmern ist erst seit Beginn der 1980-er Jahre in die Wahrnehmung der Öffentlichkeit getreten. Noch nicht lange existiert also das Bewusstsein über den Zusammenhang von Schlaganfall und dieser Herzrhythmusstörung.
Mit der systematischen Blutgerinnungshemmung konnte die Rate für Schlaganfälle und die damit erhöhte Sterblichkeit der mit Abstand häufigsten Herzrhythmusstörung dramatisch gesenkt werden. Die medikamentöse und ganz besonders die interventionelle Behandlung mit der Katheter-Ablation können die Rhythmusstörung effektiv verhindern.

Trotzdem bleibt Vorhofflimmern mit seiner epidemiologischen Dimension (1-2% der Bevölkerung leiden an dieser Rhythmusstörung) auch weiter eine große Herausforderung unserer Zeit – für die betroffenen Patienten und deren Angehörige wie auch die Gesundheitssysteme.
Vorhofflimmern ist nicht ungefährlich. Aktuelle Studien zeigen, dass Vorhofflimmern nicht nur die Lebensqualität mindert sondern vermehrt zu Herzschwäche, Demenzerkrankungen und statistisch zu früherem Tod führen kann.
Aus diesem Grund ist die Behandlung des Vorhofflimmerns auch bei scheinbar nicht oder wenig symptomatischen Formen frühzeitig indiziert.
In unserer Broschüre „Leben mit Vorhofflimmern“ finden Sie weiterführende Informationen zur Entstehung, Symptomen, Verlauf und die Basisbehandlung dieser Herzrhythmusstörung.
Die Blutgerinnungshemmung ist – entsprechend des individuellen Risikos für einen Schlaganfall – die Basisbehandlung des Vorhofflimmerns und dient zur Vorbeugung für die Entstehung von Blutgerinnseln im linken Vorhof. Diese Gerinnsel können sich bei stark eingeschränkter Pumpfunktion unter Vorhofflimmern insbesondere in einer sackartigen Ausstülpung des linken Vorhofs, im Vorhof-Ohr, bilden.
Die hohe Frequenz der elektrischen Aktivität (bis 450/min und mehr) der Vorhöfe unter Vorhofflimmen führt praktisch zum Stillstand der mechanischen Kontraktion.
Die Behandlung kann medikamentös durch leitungsverzögernde Medikamente, wie Betablocker, insbesondere bei erhöhter Grundfrequenz von über 100/min ergänzt werden. Die eigentlichen Antiarrhythmika zur Vorbeugung des Vorhofflimmerns sind bei den meisten Formen des Vorhofflimmerns nur eingeschränkt wirksam oder weisen ein hohes Nebenwirkungsprofil auf.
Deshalb hat sich in den letzten Jahren die Katheter-Ablation als effektivste und komplikationsarme Behandlungsmethode bewährt.
In Abhängigkeit vom Stadium des Vorhofflimmerns, aber auch von seiner Ursache, ist die Lungenvenen-Isolation (syn. Pulmonalvenenisolation, PVI) zwischen 60 und 80% auch längerfristig (mindestens ein Jahr) effektiv.
In unserem Zentrum und den Partnerkliniken favorisieren wir die Lungenvenen-Isolation mit der Kältetechnik (syn. Kryoablation oder Kryo-PVI) als Ersteingriff. Unserer Meinung nach ist die Kryoablation das schonendste und physiologischste Therapieverfahren, das ganz gezielt die Zellen zerstört, die zur Auslösung des Vorhofflimmerns führen, dabei aber das kardiale Bindegewebsgerüst unbeeinflusst lässt. Außerdem sind körpereigene Entzündungsreaktionen, die nach einer Ablation auftreten und wiederum selbst Vorhofflimmern auslösen können, bei dieser Energieform weniger stark ausgeprägt.
Finden Sie weiterführende Informationen zur Ablationstherapie unter Pulmonalvenen-Isolation.
Extrasystolen
Als Extrasystolen werden zusätzliche Herzschläge bezeichnet. Sie können aus den Vorhöfen (Vorhof-Extrasystolen, supraventrikuläre Extrasystolen) oder den Herzkammern (Kammer-Extrasystolen, ventrikuläre Extrasystolen) kommen.
Sowohl Vorhof- als auch Kammer-Extrasystolen verursachen eine sogenannte kompensatorische Pause, die viele Patienten als Hauptsymptom beschreiben.
Vorhofextrasystolen
In der Regel sind Vorhof-Extrasystolen ungefährlich und verursachen kaum Beschwerden. Treten sie aber sehr häufig auf (z.B. mehr als 10.000/ 24h) oder kommen als Salven vor (mehrere Extraschläge nacheinander), können sie zu deutlichen Beschwerden führen. Die Patienten klagen in diesem Fall meist über Unruhe- oder Angstgefühl, Schwindel und geringerer körperlicher Leistungsfähigkeit. Vorhof-Extrasystolen können gelegentlich Herzrhythmusstörungen wie supraventrikuläre Tachykardien auslösen.
In der Regel sind Vorhof-Extrasystolen ungefährlich und verursachen kaum Beschwerden. Treten sie aber sehr häufig auf (z.B. mehr als 10.000/ 24h) oder kommen als Salven vor (mehrere Extraschläge nacheinander), können sie zu deutlichen Beschwerden führen. Die Patienten klagen in diesem Fall meist über Unruhe- oder Angstgefühl, Schwindel und geringerer körperlicher Leistungsfähigkeit. Vorhof-Extrasystolen können gelegentlich Herzrhythmusstörungen wie supraventrikuläre Tachykardien auslösen.
Kammerextrasystolen
Auch die meisten Kammer-Extrasystolen sind in der Regel ungefährlich. Probleme gibt es – unabhängig von einer eventuellen Symptomatik – wenn bei sehr häufigen Extraschlägen die Funktion der linken Herzkammer mittel- bis langfristig geschwächt wird. Deshalb sollte nach aktuellem Erkenntnisstand bei mehr als 10.000 Extraschlägen pro Tag oder mehr als 10% der Gesamtzahl der Herzschläge zumindest eine regelmäßige Herz-Ultraschalluntersuchung erfolgen, um eine Funktionseinschränkung frühzeitig zu erkennen und eventuelle Behandlungsmaßnahmen einleiten zu können.
Die diagnostische Methode der Wahl zur Quantifizierung der Extraschläge ist das Langzeit- (Holter-) EKG. Im normalen 12-Kanal-EKG können dagegen mit einiger Sicherheit, Schlüsse zum Ursprungsort der Kammerextraschläge gezogen werden.
Einige Typen von Kammer-Extrasystolen sind darüber hinaus Symptom einer zugrundeliegenden Herzerkrankung und können prognostisch relevant sein.
So sind häufige oder gekoppelte Kammer-Extraschläge bei Zustand nach einem ausgedehnten Herzinfarkt mit schwerer Einschränkung der Funktion der linken Herzkammer Vorboten einer potentiell tödlichen Kammer-Tachykardie sein und sollten dringend weiter abgeklärt werden. Gleiches gilt für bestimmte genetische Herzerkrankungen.
Symptomatische ventrikuläre Extraschläge können in den meisten Lokalisationen bei hoher Anzahl sicher und mit hoher Effektivität durch eine Katheter-Ablation behandelt werden.
Kamertachykardien
Auch hier reicht die Bandbreite von harmlos bis hin zu lebensgefährlichen Situationen. Für keine andere Herzrhythmusstörung ist die genaue Kenntnis möglicher ursächlicher Herzerkrankungen so wichtig.
Ventrikuläre Tachykardien können aus der rechten und der linken Herzkammer kommen.
Einige besondere Formen treten im jüngeren Lebensalter auf und sind prognostisch gutartig. Trotzdem können sie zu einer ausgeprägten Symptomatik führen und eine Behandlung erfordern. Ist eine genetische, entzündliche oder muskuläre Herzerkrankung ausgeschlossen, wird meist ein Betablocker oder ein Kalziumantagonist eingesetzt. Bei Ineffektivität oder Nebenwirkungen der Medikamente kann auch bei diesen Tachykardien eine Ablation sehr effektiv helfen. Der größere Anteil dieser sogenannten idiopathischen Tachykardien (syn. „ohne Ursache“) haben ihren Ursprung im Ausflusstrakt des rechten Ventrikels, seltener des linken Ventrikels, der Aortenwurzel oder dem spezifischen Reizleitungssystem (faszikulär oder vom Purkinje-System.)
Kammertachykardien bei zugrundeliegender Herzerkrankung (nach Myokardinfarkt, nach Herzmuskelentzündung, hypertrophe und dilatative Kardiomyopathie) haben unbehandelt besonders bei eingeschränkter Linksherzfunktion mittel- bis langfristig keine gute Prognose. Eine medikamentöse Therapie ist nur begrenzt möglich, da viele Antiarrhythmika Kammertachykardien begünstigen können oder durch zahlreiche potentielle Komplikationen nicht als Dauertherapie geeignet sind.
Zur Therapie nach einer symptomatischen ventrikulären Tachykardie bei einer Auswurffunktion der linken Herzkammer ≤35 % aber auch zur Vorbeugung wird meistens ein implantierbarer Defibrillator (ICD, implantierbarer Cardioverter-Defibrillator) eingesetzt. Eine Ablationsbehandlung kann zusätzlich erforderlich sein, wenn der ICD häufiger eingreifen muss.
Kammerflimmern
Kammerflimmern ist die tödlichste der Herzrhythmusstörungen. Oft degeneriert eine ventrikuläre Tachykardie in ein potentiell tödliches Kammerflimmern. Deshalb werden beide Herzrhythmusstörungen hinsichtlich ihrer Bedeutung auch gern zusammenbetrachtet. Primäres Kammerflimmern (ohne vorangegangene ventrikuläre Tachykardie) ist wahrscheinlich selten und wird gelegentlich durch eine ganz spezifische Form ventrikulärer Extrasystolen aus dem spezifischen Reizleitungssystem ausgelöst.
Ventrikuläre Tachykardien können aus der rechten und der linken Herzkammer kommen.
Einige besondere Formen treten im jüngeren Lebensalter auf und sind prognostisch gutartig. Trotzdem können sie zu einer ausgeprägten Symptomatik führen und eine Behandlung erfordern. Ist eine genetische, entzündliche oder muskuläre Herzerkrankung ausgeschlossen, wird meist ein Betablocker oder ein Kalziumantagonist eingesetzt. Bei Ineffektivität oder Nebenwirkungen der Medikamente kann auch bei diesen Tachykardien eine Ablation sehr effektiv helfen. Der größere Anteil dieser sogenannten idiopathischen Tachykardien (syn. „ohne Ursache“) haben ihren Ursprung im Ausflusstrakt des rechten Ventrikels, seltener des linken Ventrikels, der Aortenwurzel oder dem spezifischen Reizleitungssystem (faszikulär oder vom Purkinje-System.)
Die meisten Patienten, bei denen ein Kammerflimmern beobachtet werden kann, sind bereits Träger eines ICD und können durch die zeitnahe Intervention des Aggregats buchstäblich gerettet werden.
Probleme bereiten wiederholte ICD-Entladungen durch sich wiederholende Episoden von Kammerflimmern. Für diese Gruppe der Patienten konnten wir in den letzten Jahren eine hocheffektive Ablationsbehandlung, die auf einer Modulation des Purkinjesystems basiert, entwickeln.
Therapie von Herzrhythmusstörungen
Therapie
Herzschrittmacher
Herzschrittmacher sind kleine Geräte, die in der Regel im Schulterbereich unterhalb des Schlüsselbeins implantiert werden und über ein, zwei oder drei Sonden (syn. Elektrodenkabel) mit dem Herzen verbunden sind und den Herzrhythmus kontrollieren.
Typen
Entsprechend der zugrunde liegenden Störung werden die folgenden Typen verwendet.
Einkammer-Schrittmacher
Hier werden elektrische Impulse über ein Kabel an eine Herzkammer – meistens der rechten Hauptkammer, selten den rechten Vorhof – geleitet. Die Haupt-Indikationen zur Implantation eines Einkammer-Schrittmachers sind Bradykardie bei permanentem Vorhofflimmern oder selten auftretende Pausen der Erregungsbildung oder Überleitung.
Zweikammer-Schrittmacher
Zweikammer-Schrittmacher werden von allen Typen heutzutage am häufigsten implantiert. Der Impulsgenerator ist über zwei Schrittmacher-Elektroden mit dem rechten Vorhof und der rechten Hauptkammer verbunden. Zweikammer-Herzschrittmacher können perfekt den natürlichen Erregungsablauf und die Kontraktionsdynamik des Herzens nachbilden. Deshalb nennt man sie auch physiologische Herzschrittmacher.
Dreikammer-Herzschrittmacher (syn. Biventrikuläre Herzschrittmacher, kardiale Resynchronisationstherapie)
Bei einigen Formen der Herzschwäche ist die elektrische Aktivierung der beiden Hauptkammern gestört, was zu einer Verstärkung des Verlustes an effektiver Schlagarbeit führt. Durch die synchronisierte, zeitlich gut abgestimmte Stimulation über einen Dreikammer-Herzschrittmacher kann die Herzarbeit wieder effizienter ablaufen, was zu einer deutlichen Verbesserung in der Leistungsfähigkeit dieser Patienten führt.
Moderne Schrittmachersysteme bestehen aus zwei Komponenten:
• dem Impulsgenerator, der sich aus der Batterie und dem elektronischen Steuerelement zusammensetzt und durch eine Kapsel wasserdicht und vor mechanischen Irritationen geschützt ist
• den Schrittmacher-Sonden, flexible isolierte Kabel, die über kleine Schraubmechanismen oder Anker mit der Innenseite des Herzens verbunden werden. Einige Einkammer-Schrittmacher benötigen diese Kabel nicht mehr (sogenannte „leadless pacemaker“), deren Einsatz gegenwärtig auf Patienten mit einem erhöhten Risiko für eine Schrittmacher-Infektion oder sehr betagte Patienten beschränkt ist.
Herzschrittmacher haben eine mittlere Laufzeit von mindestens 5 bis zu 12 Jahren. Bei einem Aggregatwechsel infolge einer Batterie-Ermüdung wird nur der Impulsgenerator getauscht, die Elektroden halten optimaler Weise ein Leben lang.
Eine Herzschrittmacher-Implantation ist ein relativ häufiger Routineeingriff mit einer sehr hohen Effektivität und geringem Risiko. Die kleine Operation dauert in der Regel zwischen 20 Minuten (Einkammer-Systeme, Aggregatwechsel) und 2 Stunden (Dreikammeraggregate).
Eine milde Sedierung und eine sorgfältige Lokal-Anästhesie reichen in der Regel völlig aus. Viele Herzschrittmacher-Implantationen sind auch ambulant ohne erhöhtes Risiko möglich.
Nach einer Herzschrittmacherimplantation ist das System in der Regel nach etwa 4 Wochen gut eingeheilt. Körperliche Aktivitäten auch mit den Armen sind ohne Einschränkung wieder möglich.
Komplikationen bei einer Herzschrittmacher-Implantation treten selten auf, sollten aber natürlich ernst genommen werden. Dazu gehören:
• Sondendislokation: Ein „Verrutschen“ der implantierten Elektroden ist in den Stunden und wenigen Tagen nach der Implantation das häufigste Risiko. Bei etwa 3-4% der Herzschrittmacherimplantationen ist eine Re-Operation mit erneuter Fixierung der dislozierten Sonde notwendig.
• Herzbeuteltamponade: kann durch Vermeidung einer Sonden-Positionierung in einer vulnerablen Position (rechtsventrikuläre Herzspitze, Seitenwand des rechten Vorhofs) deutlich verringert werden.
• Pneumothorax: Durch die Punktion der zum Herzen führenden Vene (V. subclavia, Schlüsselbeinvene) kann gelegentlich die Lunge verletzt werden, was zu Ansammlung von Luft im Brustraum und behinderter Atmung führt.
• Hämatom im Bereich der Implantationsstelle besonders unter bestimmten blutverdünnenden Substanzen.
• Infektion des Schrittmachersystems (bis zu 1%): Neben einer peniblen Asepsis in einem sterilen operativen Umfeld spielt die Zeitdauer einer Schrittmacher-Implantation eine große Rolle (je kürzer die Implantationsdauer um so geringer ist das Risiko einer Schrittmacherinfektion).
Kann eine Herzschrittmacherimplantation die Lebensqualität verbessern?
Durch die Schrittmacherimplantation sollten sich die durch einen zu langsamen Herzschlag ausgelösten Symptome – Schwindel, Synkopen, Leistungseinschränkung – schnell verbessern.
Moderne Schrittmachersysteme ermöglichen ein aktives Leben mit ungehinderter körperlicher Aktivität. Abgesehen von Kampf- und Extremsport mit hohem Risiko für die mechanische Schädigung des Schrittmacheraggregats, ist fast alles möglich. Fragen Sie bei seltenen Hobbies trotzdem noch einmal Ihren behandelnden Kardiologen.
Kontrollen des Schrittmachersystems sollten ein- bis zweimal jährlich durchgeführt werden. Die Intervalle richten sich u. a. nach den individuellen technischen Parametern, zusätzlichen anderen Erkrankungen oder eventuellen Herzrhythmusstörungen.
Kontrollen beinhalten eine körperliche Untersuchung insbesondere der Schrittmachertasche, der Abfrage des Ereignisspeichers des Schrittmachers, den Eigenrhythmus des Patienten, den Batteriestatus und verschiedene technische Parameter bezüglich der Kopplung des Aggregats zum Herzgewebe.
Defibrillator (ICD-) Therapie
Ein implantierbarer Kardioverter-Defibrillator (ICD) ist etwas größer als ein Herzschrittmacher, wird aber ähnlich wie dieser im Schulterbereich unterhalb des Schlüsselbeins implantiert. Das Gerät erkennt und behandelt potentiell lebensgefährliche Herzrhythmusstörungen. Ein ICD überwacht kontinuierlich den Herzrhythmus und gibt schnelle Stromimpulse oder einen elektrischen Schock zur Wiederherstellung des normalen Rhythmus ab.
Eine ICD-Implantation wird durchgeführt, wenn eine potentiell lebensbedrohliche Rhythmusstörung sich entweder bereits ereignet hat (Sekundärprävention) oder aufgrund einer Herzerkrankung die Wahrscheinlichkeit ihres Auftretens stark erhöht ist (Primäreprävention).

Einkammer-ICD
Hier stehen die Erkennung und Behandlung der potentiell lebensgefährlichen Arrhythmie im Fokus. Eine ICD-Elektrode wird im rechten Ventrikel implantiert.
Zweikammer-ICD
Eine zusätzliche Schrittmachersonde wird im rechten Vorhof platziert. Das ermöglicht neben der Verhinderung schneller Arrhythmien auch eine physiologische Stimulation wie bei einem Zweikammer-Schrittmacher.
Dreikammer-ICD (biventrikulärer ICD, kardiale Resynchronisationstherapie mit ICD)
Dieses System wird adäquat zu einem Dreikammer-Schrittmacher bei Patienten mit desynchronisierter Kontraktion von rechter und linker Kammer und einem erhöhten Risiko für maligne Herzrhythmusstörungen eingesetzt.
Ein subkutaner ICD (S-ICD) ist ein System, das ohne Sonden im Herzen auskommt. Diese Geräte werden überwiegend zur Prophylaxe lebensgefährlicher Herzrhythmusstörungen eingesetzt. Eine chronische Schrittmacherstimulation ist mit diesem Gerätetyp nicht möglich.
Die häufigsten Indikationen für eine ICD-Implantation
• Herzschwäche bei koronarer Herzerkrankung – insbesondere nach Herzinfarkt
• Herzmuskelerkrankungen mit Herzschwäche (dilatative und hypertrophe Kardiomyopathie)
• Genetische Herzerkrankungen mit erhöhtem Risiko für einen plötzlichen Herztod (Brugada-Syndrom, long oder short QT-Syndrom)
Vorbereitung, Implantation und Nachsorge ähneln der der Schrittmacherimplantation. Auch die im Zusammenhang mit der kleinen Operation verbundenen Risiken sind ähnlich.
Katheter-Ablation
Die Ablationsbehandlung ist eine minimal invasive Prozedur, die Mediziner nutzen, um anormales Gewebe zu zerstören. Bei einer Katheter-Ablation wird über einen Katheter Energie an das Gewebe übertragen, was zu einem Funktionsverlust (Erregungsbildung oder Erregungsleitung) der Zellen im Wirkbereich führt.
Die Katheter-Ablation von Herzrhythmusstörungen ist ein noch relativ junges medizinisches Behandlungsverfahren.
In der modernen Elektrophysiologie finden verschiedene Energieformen ihren Einsatz:
• Hochfrequenzstrom (syn. Radiofrequenzstrom, HF- oder RF-Strom)
• Kälte (syn. Kryoablation)
• Elektro-Vaporation
• Laser
Unter lokaler Anästhesie und allgemeiner Sedierung („Schlafnarkose“) werden über ein Blutgefäß in der Leistenregion Zugänge (Schleusen) platziert, über die ein bis drei (selten mehrere) dünne Katheter in das Herz vorgeschoben werden.

Die Katheter ermöglichen die Ableitung elektrischer Signale aus verschiedenen Herzhöhlen mit einer hohen Präzision im Bereich weniger Millisekunden. Durch elektrische Stimulation können die physiologischen und pathophysiologischen Leitungseigenschaften des Herzmuskels und des spezifischen Reizleitungssystems charakterisiert und eventuelle Herzrhythmusstörungen ausgelöst, beziehungsweise beendet werden. Oft kann durch die Gabe kurzwirksamer Medikamente die Auslösbarkeit von Arrhythmien zusätzlich beeinflusst werden.
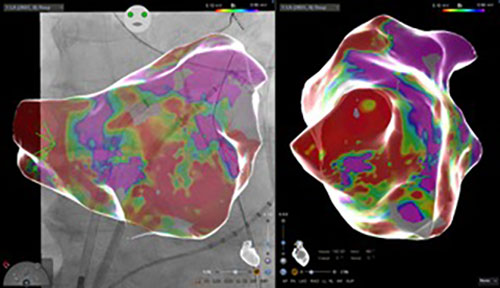
Ist die Herzrhythmusstörung charakterisiert und lokalisiert, werden ein bis mehrere Energieimpulse abgegeben. Je nach Lokalisation der Rhythmusstörung und nach Art des elektroanatomischen Substrats wird entweder der Fokus mit dem anormalen Gewebe ausgeschaltet (direkte Ablation) oder über lineare Narben“straßen“ die Ausbreitung der Erregung innerhalb eines definierten Erregungskreislaufs blockiert (indirekte Ablation).
Eine Ablationsbehandlung kann, in Abhängigkeit von der zugrundeliegenden Rhythmusstörung, eine Effektivität von nahezu 100% erreichen. Bei Herzrhythmusstörungen mit definierter und wenig variabler Elektroanatomie (AVNRT, Vorhofflattern, AV-Knoten) ist diese Effektivität auch nach Jahren unverändert hoch.
Dagegen sind Herzrhythmusstörungen bei sich veränderndem Substrat wie bei Vorhofflimmern und Kammertachykardien oft nicht ganz so effektiv behandelbar und brauchen nicht selten mehrere Eingriffe.
Eine Katheter-Ablation ist nicht selten ein komplexer Eingriff und kann im Extremfall mehrere Stunden dauern. Mit Erfahrung und guter periprozeduraler Organisation sollte die Behandlungszeit für die meisten Eingriffe zwischen 45 und 90 Minuten liegen.
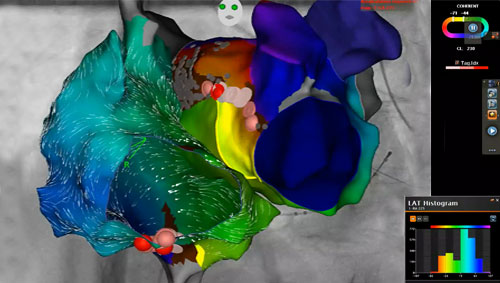
Komplikationen
Wie bei jedem medizinischen Eingriff sind Komplikationen möglich. Ein sicheres und erprobtes Präventions- und Behandlungsmanagement ist ein wichtiger Bestandteil der verantwortungsbewussten Tätigkeit des Elektrophysiologen.
In unserer eigenen Behandlungsdokumentation findet sich eine Gesamtkomplikationsrate von unter 1% auch für hochkomplexe Prozeduren. Jeder unserer Patienten wird im eingehenden Aufklärungsgespräch auch über die möglichen Risiken und Komplikationen ebenso wie über den organisatorischen und technischen Ablauf der Intervention aufgeklärt.
Pulmonalvenenisolation
Die Behandlung des Vorhofflimmerns durch Isolation der Lungenvenen existiert seit dem Ende der 90-er Jahre.
Die entscheidende Rolle für den Aufschwung dieser katheter-basierten Therapie spielte die Entdeckung, dass Extraschläge von versprengten Herzmuskelzellen in den herznahen Lungenvenen, Vorhofflimmern auslösen können. Die Verödung bzw. Isolierung dieser Zellen verhindert deutlich effektiver das Wiederauftreten von Vorhofflimmerepisoden als antiarrhythmische Medikamente.
Das Verfahren ist inzwischen sicher und effektiv durchführbar, benötigt aber ein erfahrenes Untersucherteam, eine perfekte periprozedurale Organisation und ein solides Komplikationsmanagement.

Wir verwenden die Kryo-Ballontechnik als Ablationsverfahren für alle Ersteingriffe bei einer Katheter-Ablation von Vorhofflimmern.
Vorteile der Kryo-Ballonablation sind:
• Schonendes, physiologisches Verfahren, bei dem nur die Zellen zerstört werden, die für die Auslösung des Vorhofflimmerns relevant sind (wasserreiche Muskelfasern) und das Stütz- und Bindegewebe erhalten bleibt
• Geringere Wahrscheinlichkeit von körpereigenen Entzündungsreaktionen im Ablationsbereich, die wiederum Vorhofflimmern auslösen können
• Sicheres Verfahren mit geringer Komplikationsrate und hoher Effektivität
• Geringe Prozedurzeit (90% der Prozeduren <60 min)
• Gute Reproduzierbarkeit
• Geringe Röntgenstrahlenbelastung für Patienten und Untersuchungsteam
Für eine PVI wird in Deutschland eine Klinik-Übernachtung gefordert. Durch moderne Wundverschlusstechniken sind Komplikationen im Bereich der Zugänge im Leistenbereich (fast ausschließlich rechts) sehr selten geworden.
Die Patienten können schon wenige Stunden nach der Intervention aufstehen. Körperliche Belastungen wie Sport, schweres Heben, lange Spaziergänge oder Wanderungen sind für etwa 7-10 Tage nicht empfehlenswert.
Vorhofflimmer-Rezidive unmittelbar nach der Pulmonalvenenisolation sind keine Seltenheit und können durch körpereigene inflammatorische Reaktionen, die man bis zu 12 Wochen nach dem Eingriff beobachten kann, ausgelöst. Eine erneute invasive Behandlung (Re-PVI) ist erst bei Rezidiven nach 3 Monaten indiziert und sollte dann dringend durchgeführt werden. Die häufigste Ursache für erneutes Vorhofflimmern sind erholte elektrische Leitungen aus den Lungenvenen. Die anfängliche Effektivität von durchschnittlich 70% (60-85%) kann damit auf bis zu 90% gesteigert werden.
Die Effektivität einer PVI ist von mehreren Faktoren abhängig:
• Größe des linken Vorhofs
• Fibrosierungsgrad des linken Vorhofs
• Dauer eines anhaltenden Vorhofflimmerns
• Lebensalter
• Anzahl und Schwere von Begleiterkrankungen
Glossar
Ablation: Verödung von Körpergewebe mit dem Ziel Fehlfunktionen zu behandeln
Adrenerge Substanzen: Stresshormone wie Adrenalin oder Noradrenalin
AV-Knoten: Atrioventrikulär-Knoten – kompaktes ca. 5x3x1 mm großes Gebilde aus spezialisierten Herzmuskelzellen
Bradykardie: langsamer Herzrhythmus, formal <60/min
Brugada-Syndrom: Nach den Erstbeschreibern Pedro und Josep Brugada benannte genetische Herz-Erkrankung mit gehäuften Auftreten des plötzlichen Herztodes
CRT: cardiac resynchronization therapy, kardiale Resynchronisationstherapie
DCM: dilatative Kardiomyopathie, Erkrankung des Herzmuskels mit Vergrößerung des volumens des linken Ventrikels und Einschränkung der Pumpfunktion
Faszikel, faszikulär: Teil des Reizleitungssystems der Herzkammern, Leitungsbahn aus spezialisierten, nur für die elektrische Leitung verantwortlichen Herzmuskelzellen
HSM: Herzschrittmacher
ICD: Implantierbarer Cardioverter-Defibrillator
Long-QT- und Short-QT-Syndrom: genetisch bedingte Herzerkrankung mit erhöhtem Risiko für potentiell gefährliche Kammerrhythmusstörungen, bei speziellen Formen auch bradykarde Herzrhythmusstörungen
PVI: Pulmonalvenenisolation
Purkinje-System: netzartiges Geflecht der Endstrecke des spezialisierten Reizleitungssystems der Herzkammern
Speicherkrankheit: oft genetisch bedingte Erkrankung des Herzen mit Einlagerung von vernetzten Kohlehydraten, Fetten, Eiweißstoffen, Eisen und anderen. Führt zur Verdickung der Herzwand und zur Funktionsminderung der Pumpkraft oder der Füllungsfunktion des Herzen
Synkope: Ohnmachtsanfall, rhythmogene Synkope: Bewusstlosigkeit durch Ausfall oder Unterbrechung der Impulsbildung bzw. Reizleitung
Tachykardie: schneller Herzrhythmus, formal >100/min



